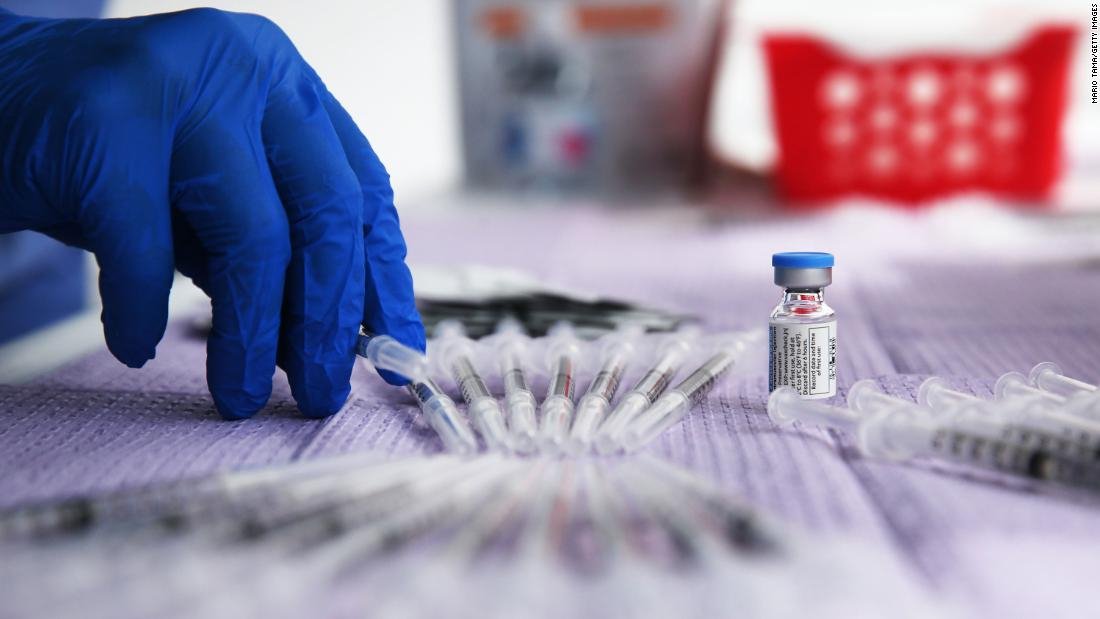
Suspenden aplicación de vacuna Johnson & Johnson en Europa y EU por posibles casos de coagulación sanguínea
Autoridades sanitarias en EU y Europa recomendaron suspender la administración del inmunizante contra el covid-19 de Johnson & Johnson por precaución ante la posible relación entre el medicamento y la aparición de coágulos sanguíneos.
La Casa Blanca aseguró que esta suspensión no tendrá un “impacto significativo” en su extensa campaña de inmunización, sin embargo, varios centros de vacunación como farmacias, supermercados y algunos consulados mexicanos anunciaron la suspensión de las jornadas de aplicación.
Por su parte, el Consulado de México en Nueva Orleans a través de un comunicado en Twitter, anunció hasta nuevo aviso la cancelación de las fechas de aplicación de la vacuna Johnson & Johnson.
El consulado mexicano de Kansas City también reportó la decisión del gobierno de pausar las inmunizaciones.
La recomendación de suspender el uso de la vacuna se dirige a quienes la estén administrando en los distintos estados, aunque por lo pronto todos los canales de salud federales que la inyectaban tendrán que detener el proceso.
Por su parte, los estados de Ohio, Nueva York, Connecticut y Nebraska, entre otros, también han suspendido la aplicación del suero.
Asimismo, la compañía anunció que retrasará la entrega de dosis a Europa, el continente más golpeado por la pandemia, que ya superó el millón de muertes desde el inicio de la crisis sanitaria.
La Administración de Drogas y Alimentos (FDA) y los Centros para el Control y Prevención de Enfermedades (CDC) están evaluando la “importancia potencial” de seis casos reportados de coágulos sanguíneos poco comunes en pacientes que recibieron la inyección, así lo comunicó la FDA a través de Twitter.
“Hasta que ese proceso esté completo, recomendamos esta pausa”, explicó.
Estos incidentes, identificados en mujeres de entre 18 y 48 años, parecen ser similares a los observados en Europa con la vacuna de AstraZeneca y ambos compuestos coinciden en que utilizan la tecnología de adenovirus como vector. Una de las pacientes falleció y otra se encuentra en estado crítico.
Esos efectos secundarios no figuraban en la lista de posibles reacciones dentro de la autorización para uso de emergencia para J&J en EU, según medios locales.